ОПРЕДЕЛЕНИЕ КЕТОНОВЫХ ТЕЛ МЕТОДОМ АБСОРБЦИОННОГО АНАЛИЗА
Секция: 4. Медицинские науки

XXV Студенческая международная заочная научно-практическая конференция «Молодежный научный форум: естественные и медицинские науки»
ОПРЕДЕЛЕНИЕ КЕТОНОВЫХ ТЕЛ МЕТОДОМ АБСОРБЦИОННОГО АНАЛИЗА
ЦЕЛЬ ИССЛЕДОВАНИЯ.
Использование оптических методов для расширения методики лабораторного анализа содержания кетонов.
ТЕОРЕТИЧЕСКОЕ ОБОСНОВАНИЕ.
Для качественного определения содержания кетоновых тел в моче в лабораторных условиях используются цветные пробы Ланге, Легаля и др.
Ряд фирм выпускает экспресс-тесты для определения кетоновых тел; определение с помощью таких тестов проводят строго по инструкции. Тест также основан на реакции Легаля. Цветная шкала сравнения на этикетке отражает концентрацию ацетоуксусной кислоты в моче. Реагент Легала — 1 %-ный раствор нитропруссида в 50 %-ном этанольном растворе 1 М NaOH.
Ацетон с нитропруссидом натрия в щелочной среде дает интенсивно-красную окраску. При подкислении уксусной кислотой окраска переходит в красно-фиолетовую:
CH3COCH3 + Na2[Fe(CN)5NO] + 2NaOH ® Na4[Fe(CN)5ON=CHCOOH3] + 2H2O
На основании известных методик лабораторного определения наличия кетонов была предложена усовершенствованная методика определения кетоновых тел в моче с помощью абсорбционного анализа.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ.
Метод абсорбционного анализа основан на способности окрашенного вещества поглощать излучение определенной длины волны, описываемой законом Бугера-Ламберта-Бера:
![]() (1)
(1)
или в логарифмическом виде:
![]() , (2)
, (2)
где: k — молярный коэффициент поглощения света;
![]() — оптическая плотность раствора;
— оптическая плотность раствора;
c — концентрация раствора;
l — толщина оптического слоя.
Определение кетоновых тел в анализируемых растворах проводили, используя следующие методики:
1 опыт:
1. Приготовили 100 мл 1 %-ного раствора нитропруссида натрия (далее НПН) Na2[Fe(NO)(CN)5] 2H2O (чда).
2. Свежеприготовленный раствор НПН поместили в 5 пробирок по 3 мл.
3. В каждую пробирку добавили по 0,1 мл 1 М раствора NaOH (хч).
4. В каждую пробирку добавили ацетон (90 %) — 0,04; 0,08; 0,12; 0,16 и 0,2 мл, соответственно.
5. На фотометре КФК-5М провели измерение интенсивности (Ui) для всех приготовленных растворов (l=540 нм) и рассчитали оптическую плотность.
В таблице 1 представлены экспериментальные результаты и данные по оптической плотности (D) приготовленных композиций.
Таблица 1.
Результаты опыта № 1
№ п/п |
Интенсивность сигнала U, В |
Оптическая плотность
|
||
U0 |
U |
U0/U |
||
1 |
2,430 |
1,811 |
1,3418 |
0,294 |
2 |
2,440 |
1,664 |
1,4663 |
0,3828 |
3 |
2,435 |
1,530 |
1,5915 |
0,4647 |
4 |
2,438 |
1,486 |
1,6406 |
0,4951 |
5 |
2,444 |
1,292 |
1,8916 |
0,6374 |
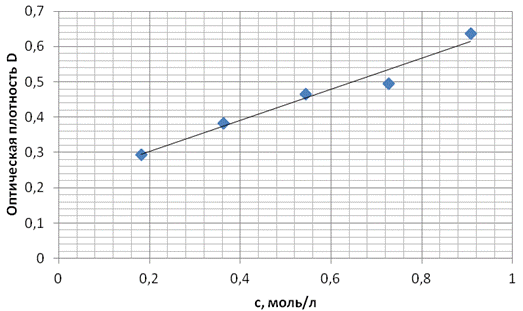
Рисунок 1. Зависимость оптической плотности раствора от концентрации ацетона (по результатам опыта № 1)
2 опыт:
1. Свежеприготовленный раствор НПН поместили в 5 пробирок по 3 мл.
2. В каждую пробирку добавили по 0,1 мл 1 М раствора NaOH (хч).
3. В каждую пробирку добавили ацетон (90 %) — 0,04; 0,08; 0,12; 0,16 и 0,2 мл, соответственно.
4. Добавили по 0,1 мл уксусной кислоты CH3COOH (9 %).
5. На фотометре КФК-5М провели измерение интенсивности (Ui) для всех приготовленных растворов (l=540 нм) и рассчитали оптическую плотность.
Таблица 2.
Результаты опыта № 2
№ п/п |
Интенсивность сигнала U, В |
Оптическая плотность
|
||
U0 |
U |
U0/U |
||
1 |
2,433 |
1,720 |
1,4145 |
0,3468 |
2 |
2,441 |
1,556 |
1,5688 |
0,45028 |
3 |
2,435 |
1,506 |
1,6169 |
0,4805 |
4 |
2,442 |
1,478 |
1,6522 |
0,5021 |
5 |
2,439 |
1,446 |
1,6867 |
0,5228 |
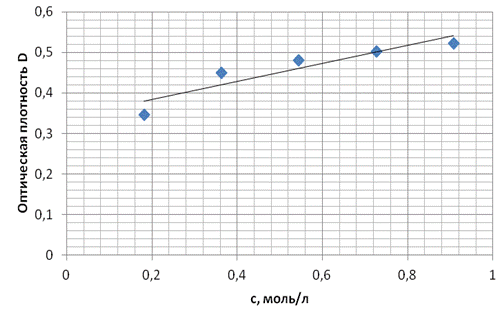
Рисунок 2. Зависимость оптической плотности раствора от концентрации ацетона (по результатам опыта № 2)
3 опыт:
1. Свежеприготовленный раствор НПН поместили в 5 пробирок по 3 мл.
2. В каждую пробирку добавили по 0,1 мл 1 М раствора NaOH (хч).
3. В каждую пробирку добавили ацетон (90 %) — 0,04; 0,08; 0,12; 0,16 и 0,2 мл, соответстенно.
4. Добавили по 0,1 мл раствора аммиака NH4OH (10 %).
5. На фотометре КФК-5М провели измерение интенсивности (Ui) для всех приготовленных растворов (l=540 нм) и рассчитали оптическую плотность.
Таблица 3.
Результаты опыта № 3
№ п/п |
Интенсивность сигнала U, В |
Оптическая плотность
|
||
U0 |
U |
U0/U |
||
1 |
2,434 |
1,581 |
1,5395 |
0,4315 |
2 |
2,339 |
0,953 |
2,4544 |
0,8979 |
3 |
2,401 |
0,670 |
3,5836 |
1,2764 |
4 |
2,444 |
0,475 |
5,1453 |
1,6381 |
5 |
2,442 |
0,184 |
13,272 |
2,5856 |
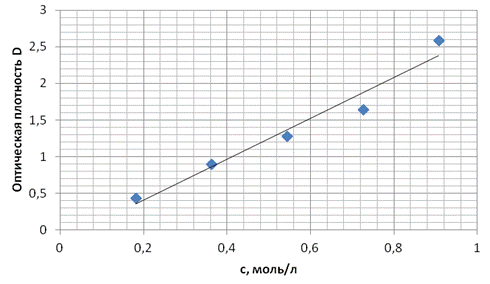
Рисунок 3. Зависимость оптической плотности раствора от концентрации ацетона (по результатам опыта № 3)
Значительное увеличение оптической плотности исследуемых композиций в присутствии аммиака (опыт № 3) происходит в ходе реакции восстановления нитропруссида натрия в щелочной среде аммиаком до пентацианоамминферрата(II) натрия:
Na2[Fe(CN)5NO] + 2NH3 + NaOH ® Na3[Fe(CN)5NH3] + N2 + 2H2O,
увеличение концентрации которого в зоне реакции изменяет окраску анализируемого раствора и повышает чувствительность рассматриваемого метода абсорбционного анализа.
ЗАКЛЮЧЕНИЕ.
1. Предложены методики построения градуировочных прямых по результатам фотометрического (абсорбционного) анализа ацетонсодержащих растворов.
2. Обнаружено значительное увеличение оптической плотности при добавлении к исходным композициям аммиака, что повышает чувствительность анализа.
Список литературы:
1. Васильев В.П. Аналитическая химия. В 2 кн.: Кн. 2: Физико-химические методы анализа: Учеб. для студ. вузов, обучающихся по химико-технол. спец. 4-е изд., стереотип. — М.: Дрофа, 2004. — 384 с.
2. Кетоновые тела в моче. Методы определения — [Электронный ресурс] — Режим доступа. — URL: http://www.clinlab.info/Ketone_bodies_in_urine.shtml (Дата обращения 15.06.2015).





